盐和酸反应的化学方程式
CaCO3+2HCl===CaCl_+H_O+CO_↑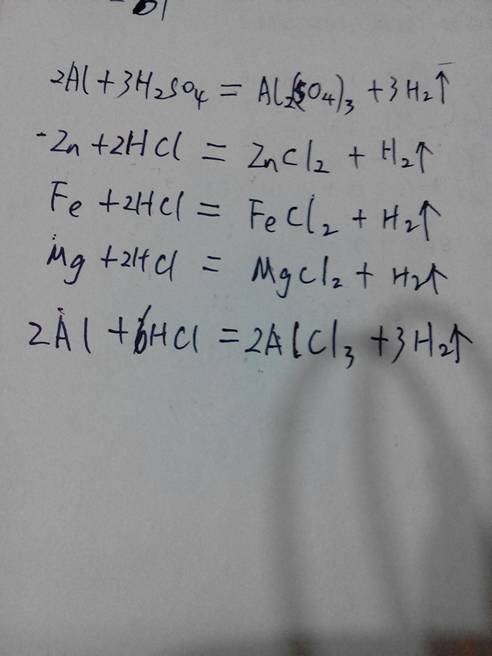
酸+盐─新酸+新盐反应物中酸必须是可溶的,盐可不可溶无所谓,生成物中至少有一种物质是气体或沉淀或水。常用的盐与酸的反应有大理石与稀盐酸反应。
如果不生成易挥发物质、沉淀物质、难电离物质等,则这种酸和盐不反应,所以酸和盐反应生成物中必有易挥发物质、沉淀物质、难电离物质中的一种。
酸与盐反应的方程式
酸与盐反应生成另一种酸和另一种盐。酸的水溶液中电离时产生的阳离子都是氢离子的化合物。可分为无机酸和有机酸。酸碱质子理论认为能释放出质子的物质总称为酸。路易斯酸碱理论认为亲电试剂或电子受体都是路易斯酸。
酸的反应
1、大理石与稀盐酸反应:CaCO3+2HCl===CaCl2+H2O+CO2↑
2、碳酸钠与稀盐酸反应:Na2CO3+2HCl===2NaCl+H2O+CO2↑
3、碳酸镁与稀盐酸反应:MgCO3+2HCl===MgCl2+H2O+CO2↑
4、盐酸和硝酸银溶液反应:HCl+AgNO3===AgCl↓+HNO3
5、硫酸和碳酸钠反应:Na2CO3+H2SO4===Na2SO4+H2O+CO2↑
6、硫酸和氯化钡溶液反应:H2SO4+BaCl2====BaSO4↓+2HCl
酸与盐反应的化学方程式
常用的盐与酸的反应有以下几种:
1、大理石与稀盐酸反应:CaCO3+2HCl===CaCl₂+H₂O+CO₂↑
2、碳酸钠与稀盐酸反应:Na₂CO3+2HCl===2NaCl+H₂O+CO₂↑
3、碳酸镁与稀盐酸反应:MgCO3+2HCl===MgCl2+H₂O+CO₂↑
4、盐酸和硝酸银溶液反应:HCl+AgNO3===AgCl↓+HNO₂
5、硫酸和碳酸钠反应:Na₂CO3+H₂SO4===Na₂SO4+H₂O+CO₂↑
6、硫酸和氯化钡溶液反应:H₂SO4+BaCl====BaSO4↓+2HCl
扩展资料
盐分为单盐和合盐,单盐分为正盐、酸式盐、碱式盐,合盐分为复盐和络盐。其中酸式盐除含有金属离子与酸根离子外还含有氢离子,碱式盐除含有金属离子与酸根离子外还含有氢氧根离子。
复盐溶于水时,可生成与原盐相同离子的合盐;络盐溶于水时,可生成与原盐不相同的复杂离子的合盐-络合物。
强碱弱酸盐是强碱和弱酸反应的盐,溶于水显碱性,如碳酸钠。而强酸弱碱盐是强酸和弱碱反应的盐,溶于水显酸性,如氯化铁。
酸在化学中狭义的定义是:在水溶液中电离出的阳离子全部都是氢离子的化合物。由阿伦尼乌斯提出,此理论即为阿伦尼乌斯酸碱理论。
大部分的酸易溶于水中,少部分,如:硅酸,难溶于水。酸的水溶液一般可导电,其导电性质与其在水中电离度有关。部分酸在水中以分子的形式存在,不导电;部分酸在水中离解为正负离子,可导电。
酸碱质子理论:较广义的定义,则认为反应中能提供质子的是酸,反之为碱,此定义称为布朗斯特(J. M. Bronsted)-劳里(T. M. Lowry)酸。此理论为酸碱质子理论。
参考资料来源:百度百科—盐
参考资料来源:百度百科—酸
酸加盐生成新酸和新盐的化学方程式是什么?
酸加盐生成新酸和新盐的化学方程式如下:
1、CaCO3+2HCl==CaCl2+H2O+CO2↑
2、Na2CO3+2HCl==2NaCl+H2O+CO2↑
3、HCl+AgNO3==AgCl↓+HNO3
4、H2SO4+BaCl2==BaSO4↓+2HCl
盐的通性
盐分为单盐和合盐,单盐分为正盐、酸式盐、碱式盐,合盐分为复盐和络盐。其中酸式盐除含有金属离子与酸根离子外还含有氢离子,碱式盐除含有金属离子与酸根离子外还含有氢氧根离子,复盐溶于水时,可生成与原盐相同离子的合盐;络盐溶于水时,可生成与原盐不相同的复杂离子的合盐-络合物。
酸和盐反应生成什么
酸+盐——新酸+新盐
条件:
①如果为碳酸盐,因为反应生成水和二氧化碳,反应很容易进行.2H++CO32—=H2O+CO2↑
②如果不是碳酸盐,反应物必须能溶于水,生成物中必须有沉淀.
扩展资料
H2SO4+BaCl2===2HCl+BaSO4(白色沉淀)
2.AgNO3+HCl===HNO3+AgCl(白色沉淀)
3.H2SO4+Ba(NO3)2===2HNO3+BaSO4(白色沉淀)
如果不生成易挥发物质、沉淀物质、难电离物质等,则这种酸和盐不反应,所以酸和盐反应生成物中必有易挥发物质、沉淀物质、难电离物质中的一种。
酸与盐反应,生成新盐和新酸有哪些化学方程式?
1.H2SO4+BaCl2===2HCl+BaSO4(白色沉淀)
2.AgNO3+HCl===HNO3+AgCl(白色沉淀)
3.H2SO4+Ba(NO3)2===2HNO3+BaSO4(白色沉淀)